60%胃癌患者迎来希望!恒瑞、信达新药成果亮相《Nature Medicine》,CLDN18.2靶点检测渐成临床刚需
2025年7月16日,国际顶级医学期刊《Nature Medicine》(影响因子58.7)同时发表了两项来自中国的突破性研究——中山大学肿瘤防治中心徐瑞华教授团队领衔的靶向CLDN18.2抗体偶联药物(ADC)SHR-A1904,以及北京大学肿瘤医院沈琳教授团队开发的创新ADC药物IBI343,双双在晚期胃癌/胃食管结合部癌治疗中取得重大进展。
这两项研究针对的是中国高发且凶险的癌种:胃癌。数据显示,中国胃癌年新发病例超35万,死亡人数逾26万,多数患者确诊时已属晚期,治疗手段有限且预后不佳。尽管免疫治疗和靶向治疗为部分患者带来希望,但现有的主流靶向药物适用人群仅占10%-15%。巨大的未满足临床需求,让医学界将目光投向了一个新兴靶点——CLDN18.2(紧密连接蛋白18.2)。
1、靶点突破:从“潜力新星”到“临床刚需” CLDN18.2是一种在正常情况下“深藏”于胃黏膜上皮细胞连接处的特殊蛋白。当细胞发生恶性转化时,这种蛋白会异常暴露在肿瘤细胞表面,成为精准打击癌细胞的“靶标”。
其在胃癌中的阳性率高达60%-80%,远超过HER2等传统靶点。尤其在中国这个胃癌高发国——年新发病例超35万,死亡26万,且多数确诊时已丧失手术机会,这一靶点的价值不言而喻。
“胃癌治疗的优势人群占比偏低——dMMR、PD-L1及HER2的阳性率分别仅约5%、50%和15%。”徐瑞华教授指出,“开发覆盖广谱人群的靶点,是当前破局的关键”。2024年底,全球首款CLDN18.2单抗药物上市,标志着该靶点正式从实验室走向临床。而如今ADC药物的加入,正为这一靶点治疗版图添上关键拼图。
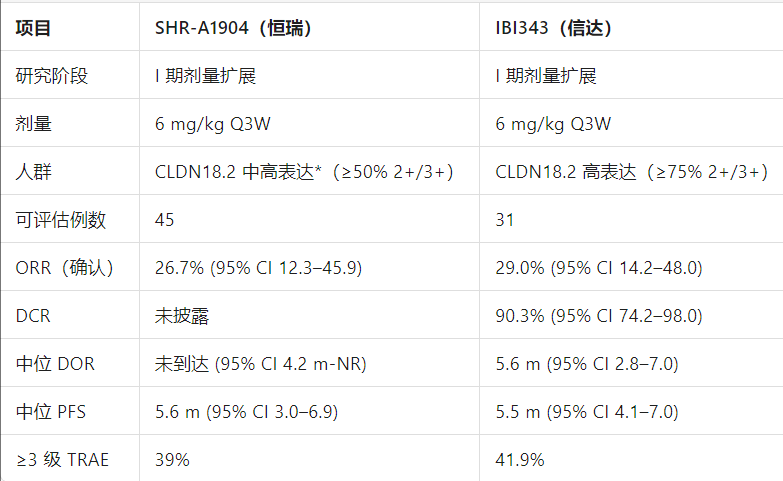
2、中国方案:双星闪耀,各展锋芒 1.恒瑞医药SHR-A1904:耐药患者的“破冰船”创新设计:由靶向CLDN18.2抗体+DNA拓扑异构酶I抑制剂(非传统微管抑制剂)+可切割连接子组成,避免与常用化疗交叉耐药17
临床突破:在纳入95例经治患者的I期试验中,69.5%患者已接受≥2线治疗。结果显示:
6.0 mg/kg组确认客观缓解率(ORR)24.2%,中位无进展生存期(PFS)5.6个月
8.0 mg/kg组ORR 25.0%,中位PFS 5.8个月
关键发现:即使既往接受过CLDN18.2靶向治疗的患者,仍能获益137
安全性:虽62.1%患者发生≥3级不良反应(常见贫血、恶心),但无治疗相关死亡,总体可控
2.信达生物IBI343:高效低毒的“精准导弹”
技术亮点:采用糖基化位点特异性偶联技术,搭载拓扑异构酶抑制剂exatecan,并创新性设计Fc沉默结构(降低胃肠道毒性)46
疗效数据:在127例患者的I期试验中,6 mg/kg组结果尤为突出:CLDN18.2高表达患者确认ORR达29%,疾病控制率90.3%中位PFS 5.5个月(较传统三线化疗提升175%)
安全性:≥3级胃肠道不良事件仅2.6%,远低于同类药物
3、未来:Claudin18.2联手免疫治疗—抗癌“双刀流” 除了单药治疗,CLDN18.2靶向药物与免疫治疗的联合也展现出前景。一项名为givastomig的药物(一种高度有效的CLDN18.2单克隆抗体)联合nivolumab(PD-1抑制剂)和化疗的Ⅰb期研究结果引人注目。
在HER2阴性、CLDN18.2阳性(≥1%)的胃癌患者中,该联合方案的客观缓解率达71%。在PD-L1高表达(CPS≥5)患者中,缓解率高达82%。
重要的是,这种联合方案耐受性良好,没有出现明显的胃肠道、肝脏或免疫相关毒性。研究还观察到,在CLDN18.2表达低于75%的患者中,缓解率也达到了80%,表明该方案适用于广泛CLDN18.2表达水平的患者。荣昌生物的Claudin18.2 ADC(RC118)正在开展与PD-1单抗的联合疗法研究,旨在评估其在Claudin18.2表达阳性的晚期恶性实体肿瘤患者中的安全性、耐受性和初步疗效。此外,礼新医药的Claudin18.2 ADC(LM-302)也与PD-1单抗或PD-1/VEGF双抗进行了联合疗法的临床试验。
2025版《CSCO胃癌指南(征求意见稿)》已将CLDN18.2检测从II级推荐升至I级推荐。
最新流调显示:亚洲胃癌组织中CLDN18.2高表达(≥75%2+/3+)比例35%–42%,与HER2阴性人群高度重叠,理论上可覆盖传统“无靶可靶”患者。
胃癌治疗领域正处于一个转折点。CLDN18.2靶点在胃癌治疗领域的重要性愈加凸显,现有的CLDN18.2单抗虽已获批,但抗体-药物偶联物(ADC)因其精准递送细胞毒性药物的特性,正为这一靶点治疗版图添上关键拼图。
